728x90
반응형
SMALL
우리가 잘 알고 있는 pH는 potential of hydrogen의 약자입니다. pH가 낮을수록 산성, pH가 높을수록 염기 성질을 가지게 됩니다.
pH는 어떻게 계산할 수 있을까요?
헨더슨-하셀발흐 식 (Henderson-Hasselbalch equation)으로 계산이 가능합니다.
Ka 이온화 상수 값이 크면 pKa가 작아지기 때문에 pH가 작아집니다.

pH 하면 빠질 수 없는 게 공통 이온 효과이지요. (common ion effect)
즉, 아래 그림처럼 공통된 하나의 이온을 가지면 평형의 이동이 일어나게 됩니다.

문제를 하나 풀어봅시다.
0.1M CH3COOH가 있다고 합시다. pH는 얼마일까요?
Ka=0.02로 가정
풀이:
아래 그림처럼 초기 값에 따라 이온화된 물질의 mol을 계산할 수 있습니다. 얼마가 있을 때 얼마가 변해서 어떻게 되었나라고 생각하면 됩니다.

아래 그림처럼 대입하고 계산 후 -log에 넣으면 pH가 구해집니다.
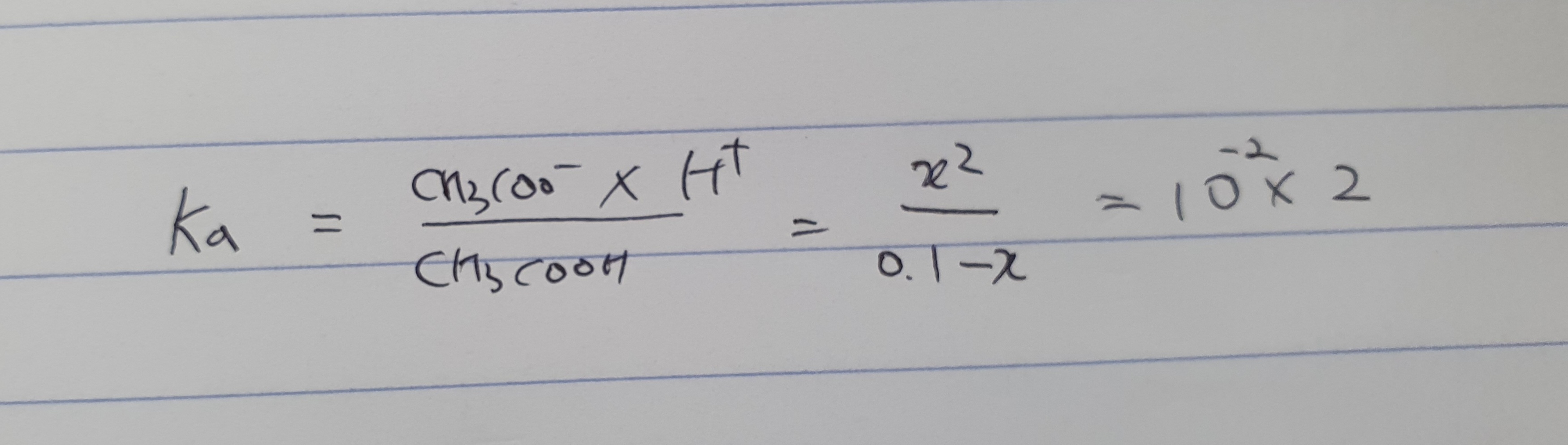
참 쉽죠?
다른 문제!
여기에 CH3COONa 0.3M을 넣으면 어떻게 될까요?
풀이:
풀이 방법은 동일합니다.
초기값, 변화값, 평형 상태로 구한 뒤 Ka 값에 대입하면 H+의 값을 구할 수 있습니다.
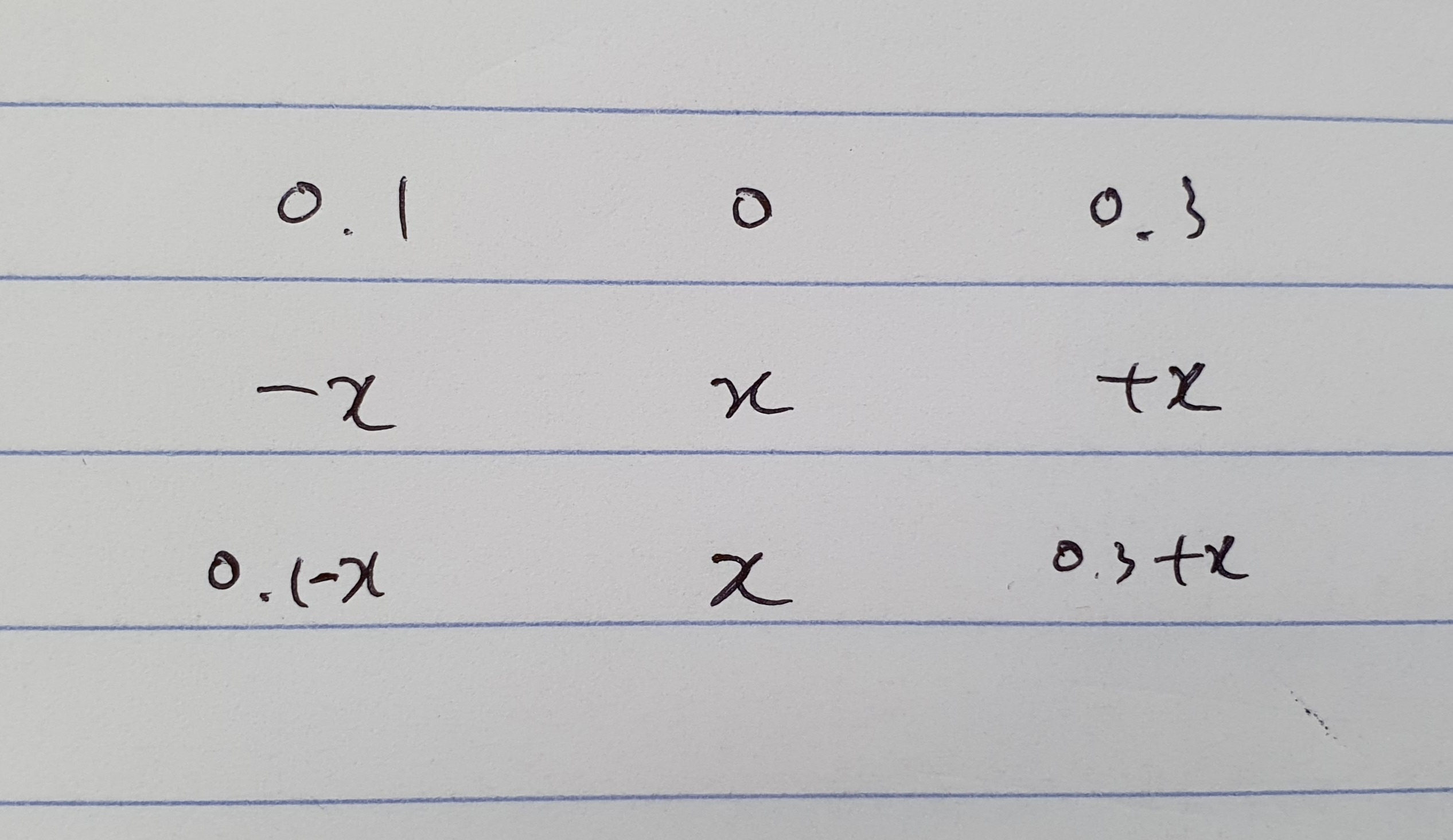
728x90
반응형
LIST
'Science Story' 카테고리의 다른 글
| 다리를 떨면 진짜 복이 나갈까? (0) | 2022.07.03 |
|---|---|
| 화학물로 폭발물을 만들 수 있다고? (0) | 2022.06.24 |
| 암모니아 생산을 위한 Haber-Bosch process (0) | 2022.05.31 |
| 몰증발열 계산법 (생각보다 아주 쉬움) (0) | 2022.05.31 |
| 물의 밀도에 관한 재미있는 사실 (0) | 2022.05.31 |



